Le propylène glycol est un élément central dans la composition des e-liquides pour cigarettes électroniques. Si le produit est connu et bien documenté scientifiquement, il reste parfois difficile pour le vapoteur de trouver des notes synthétiques à son propos et de comprendre pleinement son rôle dans la vape. Afin de proposer à ses lecteurs une information complète et structurée, le Vaping Post a demandé au Laboratoire Français du E-liquide (LFEL)* de bien vouloir exposer dans un document les généralités du propylène glycol, ainsi que son profil toxicologique.
Sommaire
Généralités sur le propylène glycol (PG)
Propriétés physico-chimiques du PG
A température ambiante, le PG a l’apparence d’un liquide légèrement sirupeux. Il ne possède ni odeur, ni goût, ni couleur. De formule brute C3H8O2, le PG a une température d’ébullition de 187° C, une température de fusion de -60° C et une masse volumique de 1,036 kg/L à 20° C.
Le PG est une molécule polaire, ses charges négatives et positives portées par les atomes ne sont pas réparties de manière homogène. Il est miscible dans l’eau et l’alcool, mais pas dans les huiles ou les solvants très apolaires (hexane, octane…). Sa polarité élevée lui permet de solubiliser de nombreuses molécules aromatiques (polaires comme : vanilline, maltol, etc.), ce qui justifie son utilisation comme support aromatique. Cependant, c’est un support inadapté pour les arômes contenant une forte concentration de molécules apolaires telles que les terpènes (limonène, pinène…).
Procédé de fabrication du PG
Le PG est issu de la carbochimie et très généralement de la pétrochimie. Il est synthétisé par la réaction d’hydratation de l’oxyde de propylène en milieu acide comme le montre la réaction suivante :
Cette réaction se déroule à 200°C et sous une pression de 12 bars. Elle produit alors un mélange de PG, de dipropylène glycol (DiPG), de tripropylène glycol (TriPG) et de petites quantités de glycols à chaine plus longue. Le mélange ainsi obtenu est déshydraté par évaporation puis chacun des glycols produits est purifié par distillation.
On notera que des travaux sont actuellement menés afin de le synthétiser par voie biologique. Mais le PG dit « bio » est une extrapolation car en réalité il n’existe pas à l’état naturel. Il peut seulement être issu, dans certains cas, de matières premières d’origine biologique.
Utilisations du propylène glycol
De nombreux secteurs industriels utilisent le PG pour ses diverses propriétés physico-chimiques dont voici quelques exemples :
- L’industrie du tabac et l’industrie cosmétique l’utilisent en tant qu’humectant antibactérien afin d’éviter la déshydratation prématurée de leurs produits. Son caractère hygroscopique lui permet de piéger les molécules d’eau environnantes. En 2009, une étude montre que sur plus de 30 000 produits d’hygiène testés (gel douche, shampooing, crème, maquillage, dentifrice, mousse à raser…), du PG est retrouvé dans plus de 28% des cas (la concentration allant de 0,0008 à 99%) [2].
- L’industrie agroalimentaire l’emploie à faible dose, comme émulsifiant (E1520) et comme support de certains arômes ou colorants.
- L’industrie aéronautique l’associe à de l’éthylène glycol pour en faire de l’antigel, pour les circuits de chauffage/climatisation des appareils. Il est important de signaler que bien que le PG soit un composant de l’antigel, il ne doit pas être confondu avec l’Ethylène Glycol (EG). Ces deux molécules sont extrêmement différentes, et contrairement au PG, l’EG est considéré comme toxique pour l’Homme. On enregistre d’ailleurs des cas d’empoisonnement voir de mortalité dus à l’ingestion d’EG [34] (volontaire ou non), alors qu’aucun cas sévère n’a été observé suite à la prise de forte dose de PG.
- L’industrie pharmaceutique y a recours en tant que support de certains principes actifs. Par exemple, on retrouve du PG dans les sprays (nasaux, buccaux) ainsi que dans certains médicaments injectés par intraveineuse [3, 4].
- L’industrie du spectacle l’utilise en tant qu’aérosol pour simuler une fumée naturelle.
- Enfin, l’industrie de la vape s’en sert comme support d’arôme et diluant pour les e-liquides.
Métabolisation du propylène glycol
La métabolisation d’une molécule par un organisme est définie par la suite de réactions chimiques que subit le composé après son absorption dans le but de l’utiliser ou de l’éliminer.
Le PG est absorbé par le corps via ingestion, inhalation ou injection (sous cutanée et intraveineuse). Sa métabolisation a lieu essentiellement dans le foie et dans une moindre mesure, dans les reins. Il se transforme alors en acide lactique et en acide pyruvique. Ces éléments, naturellement présents dans l’organisme, sont nécessaires à la production d’énergie dont le corps à besoin (cycle de Krebs). Chez un adulte en bonne santé, la majorité du PG est métabolisé ou expulsé par le corps 2 à 4h après son absorption. 12 à 45 % du PG non métabolisé est rejeté dans les urines [5-7].
A retenir :
Le PG est majoritairement issu de la pétrochimie. Il est utilisé dans de nombreux domaines industriels en raison de ses diverses propriétés chimiques et notamment de sa relative innocuité. Il est devenu un acteur incontournable de votre vie quotidienne : du dentifrice à la peinture en passant par les aliments et les médicaments, on le consomme tous les jours sans s’en rendre compte.
Toxicologie
Dans la littérature scientifique, aucun décès mettant en cause une surexposition au PG n’est répertorié. En tant qu’additif alimentaire, il est considéré comme faiblement toxique comme l’atteste sa classification par la FDA en ‘’substance GRAS’’ (Generally Recognised As Safe). L’institution précise qu’il n’y a pas de raison de suspecter un danger pour la population lors de la consommation de PG au regard des quantités consommées [8].
En se basant sur un principe de précaution, l’organisation mondiale de la santé (WHO) a fixé la dose maximale quotidienne recommandée en ingestion à 25 mg/kg. Pour une personne de 70 kg, cela représente environ 1,7 g de PG/ jour. Mais des études utilisant des doses bien plus importantes n’ont montrées aucun effet secondaire indésirable irréversible.
Cependant, une exposition à une forte quantité de PG de manière répétée et quotidienne sur une durée de plusieurs mois peut conduire à insuffisante rénale ou à une acidose lactique [5, 7,10]. Cette dernière est en fait provoquée par un excès d’acide lactique (produit de métabolisation) dans l’organisme qui induit un trouble de l’équilibre acido-basique du corps. Les symptômes associés à l’acidose lactique ne sont pas spécifiques et se caractérisent essentiellement par des douleurs diffuses thoraciques ou abdominales, des nausées ou encore des difficultés respiratoires. De même, certaines personnes seraient propices aux effets secondaires. Des maladies hépatiques ou des traitements spécifiques (médicament sur support PG) accentueraient l’accumulation de PG et donc d’acide lactique et pyruvique [11]. Toutefois, dans la plupart des cas, l’arrêt de prise du PG entraîne un retour à la normale chez les patients testés [12]. Une surexposition répétée pourrait également avoir un effet sur le système nerveux central [34].
Il est nécessaire de rappeler que ces effets sont uniquement observables dans le cadre d’études scientifiques où les sujets ont été soumis à de très fortes concentrations de PG et donc bien au-delà des quantités recommandées. Ces doses ne sont en rien comparables à celles présentes dans des produits de types agroalimentaires ou du vapotage. Par comparaison, un vapoteur inhalant 5 ml d’un e-liquide dosé à 50 % de PG est exposé à 2,5 g de PG/jour. Comme l’a dit Paracelse en 1537, ce qui fait le poison c’est la dose.
Administration par voie orale
Par voie orale, aucune étude ne mentionne de dose létale de PG chez l’Homme [16]. Dans de rares cas de surexposition non létale, la toxicité du PG n’a pas pu être mise en évidence cliniquement. Des études portant sur des effets du PG administré par gavage sur différents types d’animaux donnent peu d’effets secondaires (une baisse d’activité peut être recensée) [13-15].
Une ingestion de quantité extrême de PG serait la cause de perturbations du système nerveux (ingestion de 228 mg/kg/jour pendant 13 mois) [38]. De même, un excès d’acide lactique, dû aux effets de métabolisation d’une trop forte dose répétée de PG, engendrerait de l’acidose lactique.
Un surdosage peut également conduire à un dérèglement osmotique (déshydrations des cellules) et provoquer une toxicité cardiaque [17, 18].
Administration par inhalation
Il est possible de trouver dans la littérature scientifique, des études sur les conséquences toxicologiques de l’inhalation de PG sur des animaux et sur l’Homme.
Sur les animaux, on peut citer deux études dans lesquelles des vapeurs de PG ont été inhalées par des primates et des rats de manière journalière, pendant plusieurs mois [19,20]. Quelques effets secondaires peu sérieux ont été recensés tels que : perte ou gain de poids, saignements de nez, légère baisse du taux de globules blancs, etc. L’examen post-mortel des animaux montre qu’aucun organe n’a subi d’altérations. Une expérience similaire mais plus récente a montré des conclusions semblables [39].
Les essais sur l’Homme sont plus rares. On peut néanmoins citer une étude [21] portant sur 93 patients souffrant de désordres respiratoires chroniques. Durant 15 minutes et à l’aide d’un masque respiratoire, les sujets ont inhalé un aérosol obtenu à partir d’une solution à 40 % de PG. Les auteurs de cette étude rapportent que les patients tolèrent l’inhalation de l’aérosol sans qu’aucun effet secondaire n’ait été déclaré durant le test et dans les jours suivants. Mieux, ces chercheurs recommandent l’utilisation du PG en tant que ‘’véhicule’’ pour l’administration de drogues bronchodilatatrices en aérosol.
On peut donc comprendre que le PG, lorsqu’il est inhalé par le biais d’un e-liquide par exemple, ne présente pas de toxicité pour aucun organe y compris les poumons. Le seul effet négatif relevé est une irritation des voies respiratoires à la suite d’expositions répétées. Ce phénomène ne concernerait qu’une partie de la population qui mettrait en évidence son caractère subjectif.
Administration par contact cutané
Le PG entre dans la composition de nombreux produits pharmaceutiques et cosmétiques destinés à être appliqués sur la peau. Aussi, on recense de nombreuses études sur ces effets par contact cutané.
Dans la plupart d’entre elles, les auteurs s’accordent à dire que le PG peut provoquer une réaction de la zone traitée chez certaines personnes. Plusieurs tests de sensibilisation ou irritation cutanée ont été réalisés à partir de déodorant contenant des doses importantes de PG (jusqu’à 86 %). Sur ces différentes études, seuls quelques cas ont vu apparaître une réaction visible d’irritation [22-24].
De même, une étude menée sur 886 personnes mises en contact avec du PG pur en patch (pas de donnée sur la fréquence d’exposition) montre que 16 % des individus ont montré des signes d’irritation [25]. Parmi ces 16 %, 65 % des personnes rapportent avoir des problèmes de peau réguliers réduisant le lien de causalité entre la réaction irritante et l’exposition au PG. Les phénomènes d’irritation induits par l’exposition au PG, semblent donc être liés à la physiologie de la personne et ne semblent pas suivre un schéma applicable à l’ensemble de la population.
Une revue se basant d’ailleurs sur l’étude de plus de 45 000 personnes susceptibles d’être allergiques au PG (réaction d’eczéma due à l’application de patch contenant 20% de PG) conclut que seulement une infime partie de la population pourrait éventuellement avoir des effets secondaires liés au PG [26].
Catanzaro J.M et Smith J.G dressent en 1991 [27] une synthèse de travaux traitant de l’impact du PG sur la peau. Dans les études listées, jusqu’à 12,5 % des personnes sensibles au PG, montreraient une réaction allergique. De même, plus la population testée est exposée à de grande proportion de PG, plus le pourcentage de personnes sensibles à l’irritation du PG augmente. Ceci met en évidence une notion de « seuil » en dessous duquel il n’y aurait pas de réponse irritante. Ce seuil semble être spécifique à l’individu, soulignant le caractère subjectif de la réponse à l’exposition au PG.
Au final, la littérature s’avère contradictoire sur la nature irritante ou allergisante de cette sensibilisation. La question reste ouverte aujourd’hui, mais une majorité d’études classerait le PG comme un irritant modéré de la peau.
Administration par Intraveineuse
Des cas de surexposition au PG par intraveineuse (IV) sont répertoriés. Les chercheurs ont noté à certaines occasions, une dysfonction rénale à la suite d’injection par IV de plus de 90 g de PG [28] par jour. L’état des patients s’améliore à l’arrêt du traitement. Les études portant sur l’administration de grandes quantités de PG par IV montrent que les effets secondaires (désordres métaboliques) sont temporaires (retour à la normale après 24 à 72 heures d’arrêt du traitement) [4, 5,29].
A retenir :
Bien qu’il existe peu d’études sur l’inhalation du PG par l’Homme, de nombreuses expériences ont été réalisées sur ces effets par d’autres modes d’administration. Dans ces recherches, les doses reçues par ingestion, contact cutané ou intraveineuse sont très importantes et aucune ne provoque de conséquences irréversibles. Quant aux effets secondaires observés, ils sont dus à l’exposition de très fortes quantités de PG. À noter qu’avec un vaporisateur personnel, il est impossible d’atteindre un tel niveau d’exposition.
Le propylène glycol dans la vape (cigarette électronique)
Rôle dans l’e-liquide
Le PG est un composant de la matrice diluante utilisé dans la majorité des e-liquides commercialisés. Historiquement, c’est d’ailleurs le constituant principal de l’e-liquide. Testé et approuvé par l’industrie pharmaceutique comme véhicule de principes actifs bronchodilatateurs (ex : ventoline), il apparaît comme base idéale pour les e-liquides de part ses propriétés physico-chimiques:
Il se vaporise à relativement basse température. À l’état gazeux, il se condense en fines gouttelettes (en présence généralement d’un flux d’air) piégeant ainsi une partie des molécules voisines (i.e : nicotine, molécules aromatiques, eau, etc.). Ce phénomène rapide produit un aérosol qui imite visuellement la fumée.
Les particules liquides ou “gouttelettes” de PG formant l’aérosol, servent à diffuser les autres molécules qu’elles emprisonnent. Grâce à leur taille, ces particules de PG (de 0,1 μm à 2 μm [30]) pénètrent au plus profond des voies respiratoires [31], assurant ainsi une délivrance et une absorption presque optimale de la nicotine qu’elles contiennent.
Sa faible viscosité est bénéfique dans le cadre du mode de fonctionnement d’un vaporisateur personnel (VP). En effet, lors de la vaporisation de l’e-liquide, la mèche qui se trouve au cœur de la résistance peut s’assécher localement (au niveau de l’élément chauffant du VP). Une réhydratation trop lente de celle-ci peut provoquer un phénomène de surchauffe, entraînant une sensation olfactive et gustative désagréable appelée “dry hit”. Avec une faible viscosité (et donc une bonne capillarité), le PG limite l’assèchement local de la mèche et donc réduit le risque de dry hit.
Ses propriétés chimiques lui permettent de solubiliser parfaitement la nicotine ainsi que de nombreuses molécules aromatiques présentes dans les arômes utilisés pour la fabrication des e-liquides. Sa stabilité thermique lui permet de ne pas subir de dégradation importante lors de la vaporisation de l’e-liquide (dans des conditions normales d’utilisation). Les quelques molécules toxiques, issues de sa dégradation (principalement de la famille des aldéhydes) sont en quantité bien plus faible que dans la fumée de tabac (tableau 1) [40].
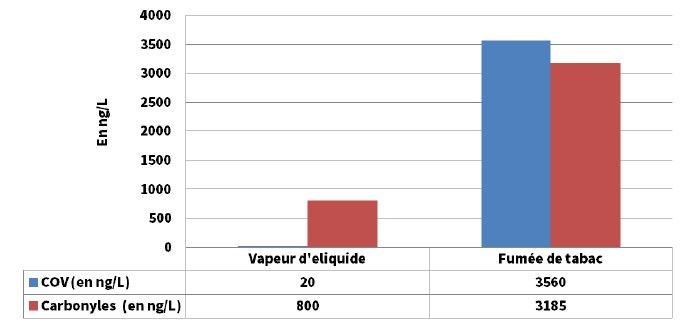
aldéhydes) retrouvés dans la vapeur d’e-liquide (50 puffs de 4 s) versus dans la
fumée de tabac (1 cigarette, puff de 2 s) [40]
Le rôle du PG dans le phénomène du “throat hit” est plus hypothétique. Cette contraction du larynx est recherchée par le fumeur et provient d’une réponse du nerf trijumeau [32, 33] (ou trigeminal nerve) à une sensation irritante ou douloureuse. C’est la nicotine qui est responsable de ce phénomène. Plusieurs suppositions peuvent être faites sur le rôle du PG : étant légèrement irritant, il pourrait favoriser la sensation de contraction. De plus, de part ses propriétés physico-chimiques, le PG est plus fluide et se vaporise plus facilement (à plus basse température) que la glycérine végétale (VG) qui est un autre support couramment utilisé par l’industrie de la vape. Ainsi, pour un même set-up (même matériel, même comportement du vapoteur), la consommation d’un e-liquide en 100% PG sera approximativement deux fois plus grande qu’un e-liquide en 100% VG (graphique 1, expériences réalisées au LFEL [41]). Ainsi, une plus grande consommation d’e-liquide, engendre naturellement une plus grande consommation de nicotine, ce qui augmente l’irritation de la gorge et donc le throat hit.

PG (en volume) dans l’e-liquide. (Les manipulations sont réalisées sur CUBIS à 1 ohm, 15 W, 1,1L/min, sur 100 puffs de 3
secondes.)
Limites et conseil d’utilisation du PG
Une des principales limites à l’utilisation du PG en tant que constituant du support diluant d’un e-liquide, concerne son caractère irritant. Son inhalation peut en effet être difficile chez des personnes qui y sont très sensibles ou intolérantes : sensation de gêne au fond de la gorge, irritation pouvant être soutenue au niveau des voies respiratoires, toux violente et répétée. Dans ce cas particulier, la seule solution semble être de s’affranchir complètement de la consommation de PG en l’excluant de la composition de l’e-liquide.
Les usagers sensibles au PG, sans en être intolérants, doivent trouver un équilibre dans la composition de la matrice diluante de l’e-liquide. Le PG a un caractère irritant à partir d’un certain seuil, il est donc recommandé au vapoteur de tester plusieurs niveaux de concentration jusqu’à trouver le dosage qui lui convient.
Il n’y a pas de composition chimique de matrice diluante “idéale”. La physiologie du vapoteur et la subjectivité des sensations perçues nécessitent une adaptation au cas par cas basée sur des critères qu’il juge importants : plaisir, risques de production d’espèces toxiques, perception des saveurs, sensibilité / insensibilité à l’irritation du PG, délivrance de nicotine, etc. L’important est que chaque usager trouve le dosage qui lui convienne pour lui permettre de quitter le tabagisme.
Il est à noter que lors d’un vapotage intensif associé à une forte consommation de PG, le caractère hygroscopique de ce dernier peut engendrer des problèmes de déshydratation comme un assèchement des muqueuses ou une sensation de sécheresse buccale. C’est pourquoi, il est conseillé de bien s’hydrater tout au long du vapotage mais également après.
De même, le PG se métabolisant dans le corps en acide lactique (vu précédemment), une consommation trop importante peut favoriser l’apparition de crampes ou de courbatures plus intenses qu’habituellement lors d’un effort physique soutenu.
Remarque : Le PG est souvent utilisé comme support diluant de certains arômes employés dans la conception d’e-liquide. L’utilisation de ces arômes introduit une quantité de PG non négligeable dans la composition finale de l’e-liquide (jusqu’à 20 % de PG dans le volume final de l’e-liquide). Sa présence comme support de l’arôme n’est souvent pas mentionnée sur les étiquettes par les marques d’e-liquide, cela pouvant relever du secret de fabrication. Néanmoins, les personnes réactives au PG peuvent accéder à ces informations en consultant les FDS des produits ou en prenant conseil auprès du fabricant lui-même.
Alternatives existantes à l’utilisation du propylène glycol
Glycérol ou glycérine végétale (VG)
Le principal composé alternatif au PG en tant que support de la matrice diluante d’un e-liquide est le 1,2,3-propanetriol, plus communément appelé glycérine végétale (VG).
Lors du vapotage, la VG se transforme en une vapeur dense et abondante. Au goût, elle est légèrement sucrée ce qui masque la perception des molécules aromatiques contenues dans l’e-liquide.
La VG possède une température d’ébullition supérieure à celle du PG (290°C). Par conséquent plus la proportion de VG dans un e-liquide est grande, plus la température nécessaire à sa vaporisation doit être élevée. Il est notable qu’une élévation de la température d’un e-liquide au moment du vapotage peut favoriser la production d’éléments de dégradation. C’est pourquoi l’analyse des émissions de vapeur est un enjeu clé pour l’avenir de la vape. Le LFEL s’attache, entre autre, à comprendre ce phénomène afin d’en mesurer les conséquences.
De plus, la VG est environ 30 fois plus visqueuse que le PG. Ainsi, elle aura plus de difficulté que le PG à imprégner la mèche du vaporisateur personnel. Il y a donc un risque d’assèchement local plus élevé. Pour pallier à ce phénomène, il faut attendre que l’e-liquide ré-imbibe correctement le dispositif et patienter quelques secondes entre deux inhalations. Le vapoteur peut également choisir d’adapter son matériel en utilisant des résistances et des mèches adaptées aux produits visqueux. Par exemple, les mèches en silice sont plus appropriées que les mèches en coton pour des liquides à forte viscosité.
1,3-propanediol
Le 1,3-propanediol est l’énantiomère du 1,2-propanediol (PG), ces deux molécules ont la même formule brute (elles sont constituées des mêmes atomes) mais ont des structures moléculaires différentes.
Plus communément appelé “végétol” dans le milieu de la vape, le 1,3-propanediol possède des propriétés physico-chimiques intermédiaires à celles du PG et de la VG. En effet, il possède une température d’ébullition de 215°C (PG : 188°C et VG : 290°C).
De plus, c’est une molécule polaire qui est donc capable de solubiliser quasiment tous les constituants retrouvés dans les e-liquides. Il constituerait un vecteur adapté à la délivrance de la nicotine comme à la perception des saveurs de l’e-liquide.
Il ressort d’une recherche bibliographique, qu’il n’y a que très peu d’études sur la toxicité du végétol en inhalation. Mais, une publication datant de 2005 (portant sur une étude [35] sur l’inhalation) rapporte que des sujets ayant inspiré 1,8 g de végétol, 6 h /jour sur une durée de 10 jours, n’ont montré aucun effet secondaire irréversible.
Au regard de cette unique étude, le végétol semble donc pouvoir être utilisé en inhalation. Il est stable thermiquement (il est employé dans la production de polyesters) [36,37] et sa dégradation thermique n’apparait qu’au-delà de 200°C. Sa vaporisation forme un aérosol similaire à celui obtenu avec du PG.
A retenir :
Le PG possède des propriétés physico-chimiques qui en font le support idéal pour la diffusion de composés comme la nicotine ou les molécules aromatiques. Il permet de délivrer la nicotine en favorisant la contraction du larynx (throat hit) tout en respectant l’équilibre aromatique de l’e-liquide. Cependant, certaines personnes peuvent être réactives ou intolérantes au PG. Aussi, il convient dans ce cas de le remplacer par de la VG ou du végétol qui possèdent des propriétés physico-chimiques proches de celles du PG. En raison du caractère subjectif des sensations souhaitées par le vapoteur, il n’existe pas de composition de matrice diluante parfaite ni universelle. Il appartient au consommateur d’e-liquide de tester plusieurs supports et dosages (PG, VG, végétol) afin de trouver le mélange qui lui convienne le mieux.
Conclusion
Le propylène glycol est utilisé depuis très longtemps dans de nombreux produits de consommation courante. Bien que peu d’études portent sur l’inhalation de PG par l’Homme dans le cadre d’une utilisation relative au vapotage, il existe beaucoup de recherches sur ses autres modes d’administration. Dans certains cas, les doses injectées (90 g / jour) sont bien supérieures à celles pouvant être inhalées quotidiennement par un utilisateur de VP. Malgré les quantités utilisées dans ces études, peu d’effets secondaires ont été observés et aucun irréversible. Dans le cadre de son utilisation par l’industrie de la vape, le PG possède plusieurs qualités qui en font est un excellent support pour les e-liquides:
- il est non toxique,
- à l’état gazeux, il se condense en fines particules pour former un aérosol efficace,
- c’est un bon support pour la nicotine et pour les arômes,
- au regard des recommandations de l’Agence européenne des produits chimiques (ECHA) le PG n’est pas considéré comme un irritant respiratoire, même si on observe parfois des intolérances,
- sa faible viscosité permet une bonne hydratation de la mèche et donc une vaporisation plus aisée.
Il est important que le consommateur trouve le mélange qui permette de sortir du tabagisme et d’en rester éloigné. La composition d’un e-liquide qu’il soit sur base PG et/ou VG et/ou végétol sera dictée par les exigences du vapoteur au regard de ses propres critères tels que sa tolérance au PG, la densité et la quantité de vapeur souhaitées, l’intensité du throat hit, ou encore la perception des saveurs aromatiques.
La composition de la base diluante d’un e-liquide peut donc être considérée comme un paramètre subjectif qu’il est nécessaire d’adapter à chaque utilisateur. Il convient néanmoins d’ajuster son comportement et son matériel aux caractéristiques de son e-liquide sous peine de favoriser la production d’éléments de dégradation toxiques dans les émissions de vapeur. Ce sujet qui est l’un des enjeux clés pour l’avenir de la vape est, depuis 2014, étudié par l’équipe de scientifiques du LFEL.
Notes et références
1: Elements of Chemical Reaction Engineering: COMSOL Models
2: Fiume et al, Int J of toxicology 31(sup2) : 245S-260S, 2012
3: Van de Weile et al, J. Neurosurg. Anesth 7(4) : 259-62, 1995
4: Demey et al. Lancet 1 : 1360, 1984
5: Wilson et al, Chest 128 :1674-1681,2005
6: Cawley et al, Pharmacotherapy 21 :1140-1144, 2001
7: Arroliga et al, Crit Care Med 32 :1709-1714, 2004
8: Select Committee on GRAS Substances (SCOGS) Opinion: Propylene Glycol and Propylene Glycol Monostearate
9: Tuohy et al, Lancet 361 :308, 2003
10: Barnes et al, Pharmacotherapy 26 :23-33, 2006
11: Zar et al, seminars in dialysis (20), 2007
12: Yaucher et al, Pharmacotherapy 23 :1094-1099, 2003
13: Christopher M.M. et al, Vet. Pathol., 27 : 299-310, 1990
14: Thackaberry E.A. et al, Toxicological Sciences 117 : 485-492, 2010
15: Enright B. et al, Birth defects Reseach Part B: dev. And repro. Tox. 89, 504-516, 2010
16: Cavender et al, Toxicology, 4645-4719, 1994
17: Ruddick et al, Toxicol Appl Pharmacol, 21 :102-111, 1972
18: Martin et al, J.Pediatr., 77 :877-878, 1970
19: Robertson, O. H. et al, J. Pharmacol. Exp. Therap., 91:52–76, 1947
20: Suber R.L. et al, Food Chem Toxicol., 27(9):573-584, 1989.
21: Cohen et Crandall, Am J Medical Sciences, 247 : 57-61, 1964
22: Tanojo et al, J controlled release 58 ;97-104, 1999
23: Menning et al, unpublished data received from the council, study dated 1998 and 1997
24: Recherches cliniques non publiées
25: Warshaw, T. G.et al, J. Invest.Dermatol., 19:423–430, 1952.
26: Lessmann, H. et al, Contact dermatitis 53, 247–59, 2005
27: Catanzaro J.M. et al, J. Am. Acad. Dermalo., 24(1): 90-95, 1991
28: Yorgin P.D. et al, Am. J. Kidney Dis., 30:134-9, 1997
29: Wilson, K. C. et al, The New England journal of medicine 343 : 815, 2000
30: McAuley et al, Inhalation Toxicology, 50(12) : 850-857, 2012
31: Joachim Heyder, Proceedings of the American thoracic society, Vol 1, 2004
32: Dautzenberg et al, Tobacco prevention and cessation, 2(april) :52, 2016
33: Megerdichian et al, nicotine and tobacco research vol 9,11 1119-1129, 2007.
34: Laking et al, critical reviews in toxicology, 29(4): 331-365, 1999
35: Scott et al, inhalation toxicology, 17:487-493, 2005
36: Chrissafis et al, polymer degradation stability 91,60-68, 2006
37: Umare et al, polymer degradation stability 92, 464-479, 2007
38 : Arulanantham K. et al, J. Pediatr. 93 :515-516, 1978
39 : Werley M. S. et al, Toxicology 287, 76-90, 2011
40 : McAuley T.R. et al, Inhalation Toxicology, 24(12) :850-857, 2012
41 : Sorin J. et al, Poster E-Cig symposium, La rochelle, 2016
* Document rédigé par le docteur Hélène LALO et Jérémy SORIN. Les propos recueillis dans ce document ne constituent pas un avis médical. En cas de doute, consultez un professionnel de santé.
Pour aller plus loin
- Notre guide sur les arômes dans les e-liquides.
- Elle permet de faire plus de vapeur, incontournanle dans les recettes pour e-liquide, nous vous expliquons tout sur la glycérine végétale.
- Vous vous posez des questions sur la nicotine ? Nous vous expliquons tout.
- Faut-il se méfier de certains e-liquides ? Des éléments de réponse avec Vincent Cuisset de la société Vincent dans les Vapes.
- Il a fait la Une des journaux il y a quelques années. E-liquide : L’absence de Diacétyle comme nouvel argument commercial ?